我国学者在揭示线粒体自噬维持心血管稳态方面取得进展
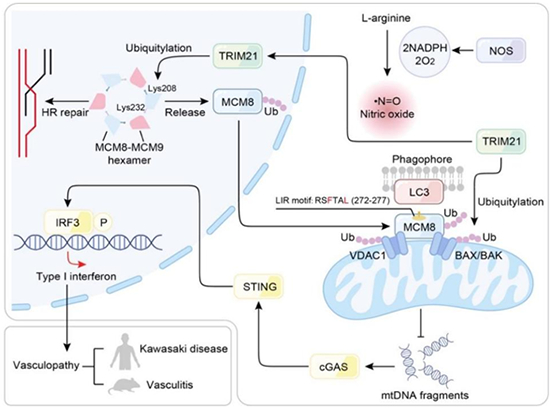
图 MCM8介导的线粒体自噬在心血管疾病中作用
在国家自然科学基金项目(批准号:82125015、92042303、81901665)等资助下,广州医科大学张玉霞、顾晓琼和重庆国际免疫中心吴玉章团队在线粒体自噬维持心血管稳态方面取得进展。研究成果以“一氧化氮通过MCM8介导的线粒体自噬在川崎病模型中的心血管保护作用(MCM8-mediated mitophagy protects vascular health in response to nitric oxide signaling in a mouse model of Kawasaki disease)”为题,于2023年8月11日在《自然•心血管研究》(Nature Cardiovascular Research)杂志上发表。论文链接https://doi.org/10.1038/s44161-023-00314-x。
川崎病也称为黏膜-皮肤淋巴综合征,是一种病因不明的急性发热性疾病,表现为系统性血管炎,是5岁以下儿童获得性心脏病的主要病因,可出现冠状动脉扩张或动脉瘤等,在中国、日本和韩国等东亚儿童中高发。但川崎病的发病机制及冠状动脉瘤发生的遗传学基础尚不清楚。
研究团队通过对健康以及川崎病患者外周血转录组学差异分析,发现在并发冠状动脉瘤的川崎病患儿中染色体维持复合体8(MCM8)基因显著降低,I型干扰素信号激活增加;通过构建敲除Mcm8的川崎病模型小鼠,发现Mcm8缺失后冠状动脉炎严重程度显著增加,冠状动脉周围组织cGAS-STING-I型干扰素等炎症信号通路显著激活,心肌线粒体排列紊乱且数量减少。机制研究发现抑制一氧化氮(NO)合成会加重川崎病动物模型的症状,NO缺乏抑制了E3泛素酶对MCM8的泛素化,造成MCM8-MCM9 复合体无法解离,阻碍MCM8在线粒体的定位而抑制线粒体自噬功能,进而激活cGAS-STING-I型干扰素通路,导致冠状动脉血管炎;激活NO通路可以促进MCM8介导的线粒体自噬,发挥心血管保护作用。研究还发现东亚人群中存在的MCM8-P276变异可引起线粒体自噬下降,导致cGAS-STING-I型干扰素通路过度激活,与川崎病的易感性有关(图)。
该研究提示通过靶向增强MCM8介导的线粒体自噬或抑制I型干扰素通路过度激活,可以改善川崎病冠状动脉炎,为川崎病的治疗提供了新思路。
