我国学者在脑卒中tPA溶栓后出血转化的机制及干预策略研究方面取得进展
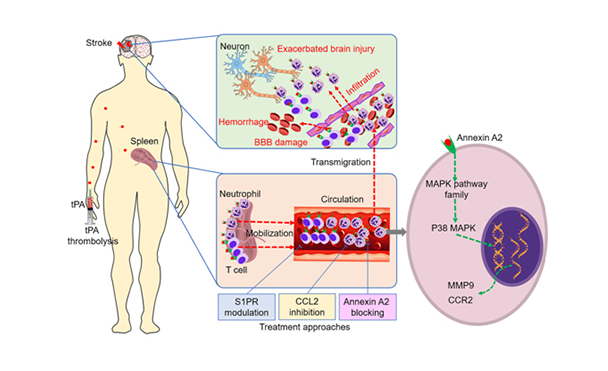
图. tPA溶栓后出血转化的免疫机制及干预策略
在国家自然科学基金项目(批准号:91642205、81830038、81701176)等支持下,天津医科大学总医院施福东团队最新研究揭示了急性缺血性脑卒中组织纤溶酶原激活剂(tissue plasminogen activator,tPA)溶栓后出血转化的机制及干预策略,研究成果以“tPA活化免疫细胞加重卒中后出血转化(tPA mobilizes immune cells that exacerbate hemorrhagic transformation in stroke)”为题,于2020年10月19日在线发表在《循环研究》(Circulation Research)杂志,论文链接https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.120.317596。
脑卒中是我国第一位致死和致残病因,其中缺血性卒中占60%~70%。tPA静脉溶栓是缺血性卒中目前唯一证明有效的急性期药物治疗方式。然而,由于狭窄的治疗时间窗(4.5小时)以及溶栓后增加的脑出血风险,仅有3%的卒中患者可以获益。溶栓后出血转化的直接原因是脑缺血后血脑屏障完整性受到破坏,血管再通使血液成分从破坏的血脑屏障进入脑实质,但是目前对血脑屏障出现严重破坏的病理生理机制并不清楚。
为解决上述问题,该团队建立了急性缺血性脑卒中tPA静脉溶栓治疗前瞻性研究队列,纵向比较了71例接受tPA静脉溶栓治疗的急性脑卒中患者溶栓前后外周血免疫细胞的变化,发现tPA治疗后外周血中性粒细胞和淋巴细胞数目快速升高。进一步在大鼠血栓栓塞性脑卒中模型中的探索表明:tPA通过结合膜联蛋白A2(annexin A2)作用于免疫细胞,调控这些细胞的转录组基因表达,迅速活化外周免疫细胞,进而加重血脑屏障破坏,促进溶栓后的出血转化。通过CC族趋化因子配体2(CCL2)抑制剂宾达利(Bindarit)抑制中性粒细胞趋化,或鞘磷脂-1-磷酸受体(S1PR)调节剂抑制外周淋巴细胞迁移,均可以显著降低溶栓后出血风险,并改善神经功能(如图)。
该研究证实精准免疫干预可能降低缺血性脑卒中接受溶栓治疗的出血转化风险,为解决这一临床难题提供了新的治疗策略。
转自:国家自然科学基因委员会
原文链接:
http://www.nsfc.gov.cn/publish/portal0/tab448/info79169.htm